Projet InnoVinFXS : La mutation derrière le syndrome de l'X-Fragile
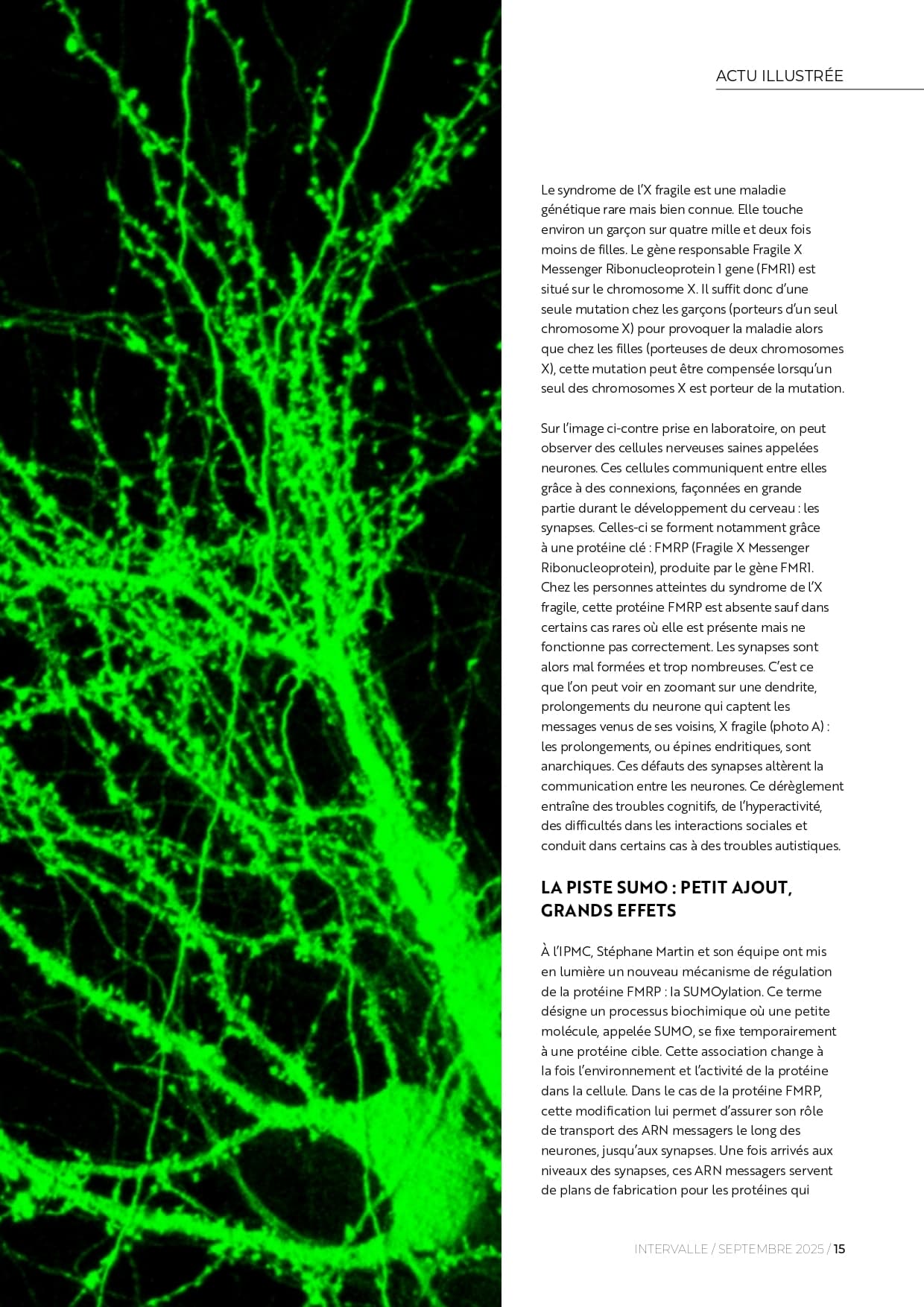
La déficience intellectuelle et les troubles du spectre autistique sont les causes majeures de handicap chez l’enfant et un enjeu essentiel de santé publique. Le syndrome de l’X-fragile est la forme héréditaire la plus fréquente de déficience intellectuelle et la première cause génétique connue de troubles du spectre autistique. Cette maladie du neurodéveloppement est due à la mutation d'un seul gène, le gène FMR1 sur le chromosome X. Cette maladie résulte donc du non fonctionnement du produit de ce gène FMR1, la molécule FMRP. Celle-ci est naturellement exprimée dans le cerveau. Elle lie et transporte des milliers d’ARN messagers, c’est-à-dire des composés (acide ribonucléique) qui portent l'information génétique nécessaire à la synthèse des protéines de la cellule, jusqu’aux sites où ces ARN seront traduits en protéines. Ces étapes sont essentielles pour établir les connexions entre les cellules nerveuses ou neurones qui composent le cerveau. L'équipe de recherche a mis en évidence un mécanisme de régulation de la fonction de transport d’ARNm de FMRP.
Ce nouveau mécanisme appelé SUMOylation, consiste en l’attachement d’une petite molécule appelée SUMO sur ces cibles, ici FMRP, ce qui permet de contrôler sa localisation et son activité dans le neurone. Les scientifiques ont identifié les sites de SUMOylation sur la molécule FMRP et démontré que leur rôle est essentiel pour contrôler la formation des connexions neuronales. De manière très intéressante, des mutations ont été retrouvées dans le génome humain qui conduisent au syndrome de l'X-fragile. Une de ces mutations, la mutation FMRP-R138Q, est située à proximité du site de SUMOylation qui régule la formation des connexions neuronales.
Le but du projet InnoVinFXS est d’identifier les conséquences fonctionnelles de cette mutation récurrente et qui est proche du site de SUMOylation de FMRP et d’envisager des solutions pour pallier aux effets négatifs induits par la mutation :
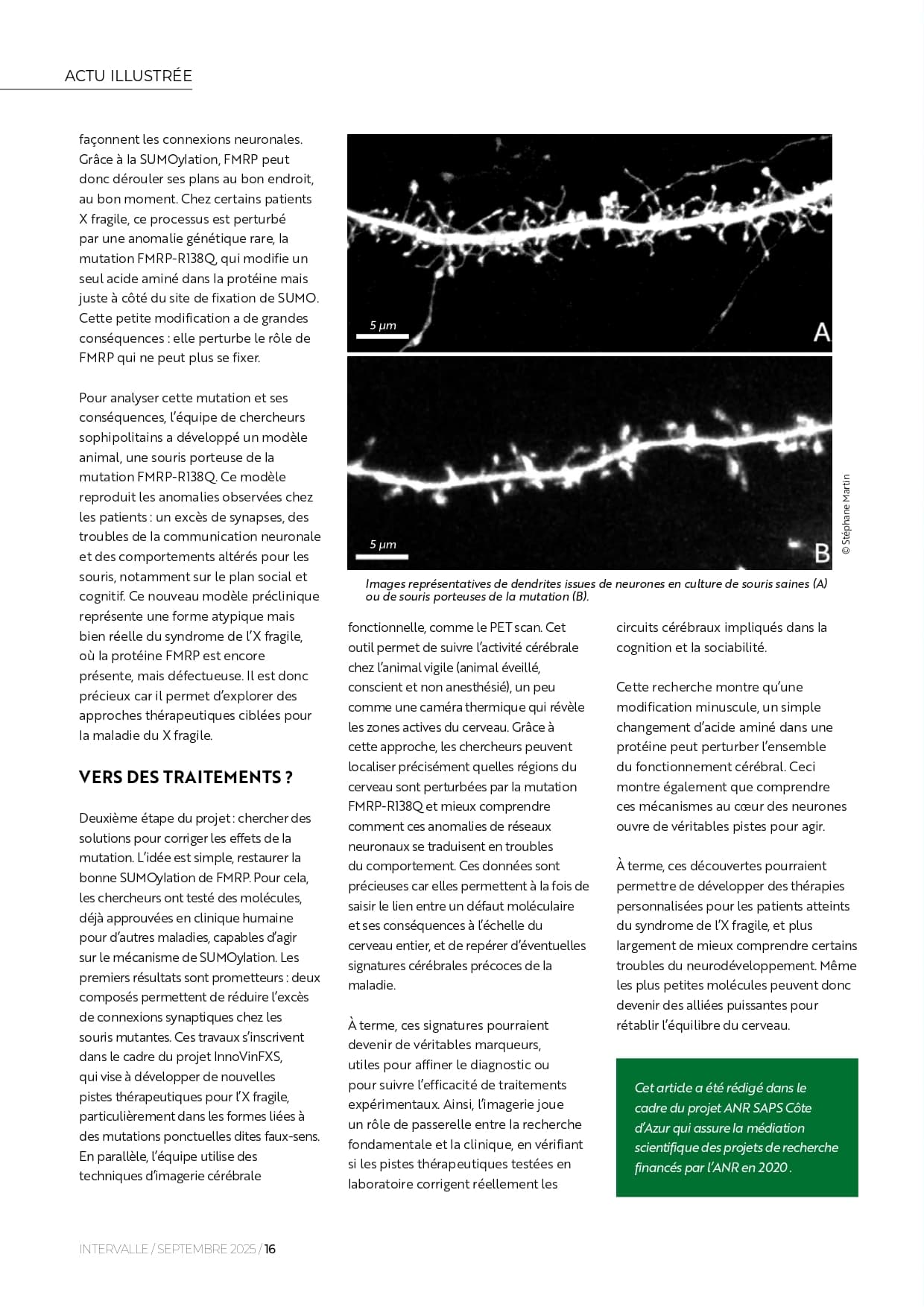
- Pour effectuer cette recherche, les chercheurs ont dû générer un modèle de la maladie portant cette mutation FMRP-R138Q. Ce nouveau modèle génétique est la souris Knock-in FMRP-R138Q. Elle porte notre mutation spécifique d’intérêt dans le gène fmr1 pour générer la protéine du X fragile FMRP-R138Q. La première partie du travail a donc été de démontrer que ce nouveau modèle était valide et récapitulait les altérations observées chez les patients atteints du syndrome de l'X fragile. Ainsi, l'équipe de recherche a démontré que la mutation FMRP-R138Q affecte l'activité et la fonction de la protéine FMRP. La conséquence directe est une augmentation importante de la quantité de connexions neuronales générée pendant le développement cérébral, ce qui conduit à des défauts de communication entre les neurones du cerveau. Les conséquences directes de ces anomalies sont des altérations de comportements socio-cognitifs c’est-à-dire, des atteintes dans les processus de mémorisation et d’interactions sociales chez la souris modèle de la maladie, de manière similaire à ce qui est observée chez les patients X fragiles porteurs de la mutation R138Q. L'équipe poursuit actuellement les investigations avec les collaborateurs pour identifier des signatures spécifiques dans le cerveau des modèles souris portant la mutation FMRP-R138Q par des approches d’imagerie fonctionnelle de type PET scan.
- La deuxième partie du projet a pour but d’élaborer des solutions pour corriger les anomalies fonctionnelles induites par la mutation FMRP-R138Q. Pour cela, l'équipe cible le mécanisme de SUMOylation afin de rétablir la capacité de FMRP à contrôler la densité de connexions neuronales qui est défectueuse dans notre modèle de souris comme chez les patients atteints de X-Fragile. Le but est ici d’employer des molécules déjà utilisées en clinique humaine pour d’autres pathologies et ciblant le mécanisme de SUMOylation afin d’évaluer leur potentiel thérapeutique sur notre modèle d’étude. Les résultats préliminaires sont encourageants puisque parmi les molécules testées, deux d’entre elles présentent des activités intéressantes en diminuant l’excès de connexions cérébrales chez le modèle FMRP-R138Q. A terme, l'équipe de recherche espérent pouvoir valider ces approches pharmacologiques sur notre modèle préclinique et ainsi élaborer des stratégies pour le développement de nouvelles pistes thérapeutiques du syndrome de l’X fragile.
Découvrez le portrait de Stéphane Martin à l'origine du projet InnoVinFXS !